Belerang
Belerang (bahasa Latin: sulphur; bahasa Inggris: sulfur atau sulphur), yang juga disebut sulfur, adalah unsur kimia dengan lambang S dan nomor atom 16. Belerang merupakan unsur nonlogam yang melimpah dan multivalen. Dalam kondisi normal, atom belerang membentuk molekul oktatomik siklik dengan rumus kimia S8. Belerang elemental adalah padatan kristal kuning cerah pada suhu kamar. Belerang adalah unsur paling melimpah kesepuluh berdasarkan massa di alam semesta dan paling banyak kelima di Bumi. Meskipun terkadang ditemukan dalam bentuk asli yang murni, belerang di Bumi biasanya terdapat sebagai mineral sulfida dan sulfat. Karena berlimpah dalam bentuk aslinya, belerang telah dikenal sejak zaman kuno, dan kegunaannya telah disebutkan pada zaman India Kuno, Yunani Kuno, Tiongkok Kuno, dan Mesir Kuno. Secara historis dan dalam literatur, belerang juga disebut sebagai brimstone,[5] yang berarti "batu yang terbakar".[6] Saat ini, hampir semua belerang elemental diproduksi sebagai produk sampingan dari penghilangan kontaminan yang mengandung belerang dari gas alam dan minyak bumi.[7][8] Penggunaan belerang komersial terbesar adalah produksi asam sulfat untuk pupuk sulfat dan fosfat, dan proses kimia lainnya. Belerang digunakan dalam korek api, insektisida, dan fungisida. Banyak senyawa belerang yang berbau, dan bau gas belerang seperti bau gas alam, aroma sigung, limau gedang, dan bawang putih disebabkan oleh senyawa organobelerang. Hidrogen sulfida memberikan bau khas pada telur busuk dan proses biologis lainnya. Belerang merupakan unsur penting bagi semua kehidupan, tetapi hampir selalu dalam bentuk senyawa organobelerang atau logam sulfida. Asam amino (dua proteinogenik: sisteina dan metionina, dan banyak nonkode lainnya: sistina, taurina, dll.) serta dua vitamin (biotin dan tiamina) adalah senyawa organobelerang yang sangat penting untuk kehidupan. Banyak kofaktor yang juga mengandung sulfur, termasuk glutationa, dan protein besi–belerang. Disulfida, ikatan S–S, memberikan kekuatan mekanik dan ketidaklarutan (antara lain) protein keratin, yang ditemukan pada kulit luar, rambut, dan bulu. Belerang adalah salah satu unsur kimia inti yang dibutuhkan untuk fungsi biokimia dan merupakan makronutrien elemental unsur untuk semua organisme hidup. Karakteristik Sifat fisikBelerang membentuk beberapa molekul poliatomik. Alotrop yang paling terkenal adalah oktasulfur, siklo-S8. Grup titik siklo-S8 adalah D4d dan momen dipolnya adalah 0 D.[9] Oktasulfur adalah padatan lembut berwarna kuning cerah yang tak berbau, tetapi sampel tak murni memiliki bau yang mirip dengan korek api.[10] Ia melebur pada 115,21 °C (239,38 °F), mendidih pada 444,6 °C (832,3 °F),[5] dan menyublim kurang lebih antara 20 °C (68 °F) dan 50 °C (122 °F).[11] Pada 95,2 °C (203,4 °F), di bawah suhu leburnya, siklo-oktasulfur berubah dari α-oktasulfur menjadi β-polimorf.[12] Struktur cincin S8 hampir tidak berubah oleh perubahan fasa ini, yang memengaruhi interaksi antarmolekul. Di antara suhu lebur dan didihnya, oktasulfur mengubah alotropnya lagi, berubah dari β-oktasulfur menjadi γ-sulfur, sekali lagi disertai dengan massa jenis yang lebih rendah tetapi kekentalan meningkat karena pembentukan polimer.[12] Pada suhu yang lebih tinggi, kekentalan menurun saat depolimerisasi terjadi. Belerang cair mengasumsikan warna merah tua di atas 200 °C (392 °F). Massa jenis belerang sekitar 2 g/cm3, tergantung pada alotropnya; semua alotrop stabil adalah insulator listrik yang sangat baik. Belerang tidak larut dalam air tetapi larut dalam karbon disulfida dan, pada tingkat lebih rendah, dalam pelarut organik nonpolar lainnya, seperti benzena dan toluena. Sifat kimiaDalam kondisi normal, belerang akan terhidrolisis sangat lambat untuk membentuk terutama hidrogen sulfida dan asam sulfat:
Reaksi tersebut melibatkan adsorpsi proton ke gugus S8, diikuti dengan disproporsionasi ke dalam produk reaksi.[13] Energi ionisasi belerang kedua, keempat, dan keenam masing-masing adalah 2252 kJ/mol−1, 4556 kJ/mol−1, dan 8495,8 kJ/mol−1. Komposisi produk reaksi belerang dengan oksidan (dan keadaan oksidasinya) bergantung pada apakah pelepasan energi reaksi mengatasi ambang batas ini. Menerapkan katalis dan/atau suplai energi luar dapat memvariasikan keadaan oksidasi belerang dan komposisi produk reaksi. Walaupun reaksi antara belerang dan oksigen pada kondisi normal menghasilkan belerang dioksida (keadaan oksidasi +4), pembentukan belerang trioksida (keadaan oksidasi +6) membutuhkan suhu 400 – 600 °C dan adanya katalis. Dalam reaksi dengan unsur-unsur dengan keelektronegatifan yang lebih rendah, ia bereaksi sebagai oksidan dan membentuk sulfida, di mana ia memiliki tingkat oksidasi –2. Belerang bereaksi dengan hampir semua unsur lain kecuali gas mulia, bahkan dengan logam iridium yang terkenal tak reaktif (menghasilkan iridium disulfida).[14] Beberapa dari reaksi tersebut membutuhkan suhu tinggi.[15] Alotrop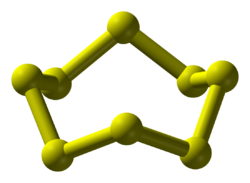 Belerang membentuk lebih dari 30 alotrop padat, lebih banyak dari unsur lainnya.[16] Selain S8, beberapa cincin lain telah diketahui.[17] Menghapus satu atom dari mahkota S8 akan memberi S7, yang lebih berwarna kuning tua daripada S8. Analisi HPLC dari "belerang elemental" mengungkapkan campuran kesetimbangan dari terutama S8, tetapi dengan S7 dan sejumlah kecil S6.[18] Cincin yang lebih besar telah dipersiapkan, termasuk S12 dan S18.[19][20] Belerang amorf atau "plastik" dihasilkan dengan pendinginan cepat dari belerang cair—misalnya, dengan menuangkannya ke dalam air dingin. Studi kristalografi sinar-X menunjukkan bahwa bentuk amorf mungkin memiliki struktur heliks dengan delapan atom per putaran. Molekul polimer melingkar panjang membuat zat kecoklatan menjadi elastis, dan dalam jumlah besar bentuk ini terasa seperti karet mentah. Bentuk ini metastabil pada suhu kamar dan secara bertahap kembali ke alotrop molekul kristal, yang tidak lagi elastis. Proses ini terjadi dalam hitungan jam hingga hari, tetapi dapat dikatalisasi dengan cepat. Isotop
Belerang memiliki 23 isotop yang diketahui, empat di antaranya stabil: 32S (94,99%±0,26%), 33S (0,75%±0,02%), 34S (4,25%±0,24%), dan 36S (0,01%±0,01%).[21][22] Selain 35S, dengan waktu paruh 87 hari, isotop belerang yang radioaktif memiliki waktu paruh kurang dari 3 jam. Kelebihan 32S dijelaskan oleh produksinya dalam proses alfa (salah satu kelas utama reaksi fusi nuklir) di dalam bintang yang meledak. Isotop belerang stabil lainnya diproduksi dalam proses bypass yang terkait dengan 34Ar, dan komposisinya bergantung pada jenis ledakan bintang. Misalnya, lebih banyak 33S yang berasal dari nova, daripada dari supernova.[23] Di planet Bumi, komposisi isotop belerang ditentukan oleh Matahari. Meskipun diasumsikan bahwa distribusi isotop belerang yang berbeda harus kurang lebih sama, telah ditemukan bahwa proporsi dua isotop belerang yang paling melimpah, 32S dan 34S, bervariasi dalam sampel yang berbeda. Pengujian rasio isotop (δ34S) ini dalam sampel memungkinkan untuk membuat perkiraan tentang sejarah kimianya, dan dengan dukungan metode lain, memungkinkan untuk menentukan usia sampel, memperkirakan suhu kesetimbangan antara bijih dan air, menentukan pH dan fugasitas oksigen, mengidentifikasi aktivitas bakteri pereduksi sulfat pada saat pembentukan sampel, atau memperkirakan sumber utama belerang dalam ekosistem.[24] Namun, diskusi tentang apa alasan sebenarnya dari pergeseran δ34S, aktivitas biologis atau perubahan pascadeposital, terus berlanjut.[25] Misalnya, ketika mineral sulfida diendapkan, kesetimbangan isotop antara padatan dan cairan dapat menyebabkan perbedaan kecil pada nilai δ34S mineral kogenetik. Perbedaan antara mineral dapat digunakan untuk memperkirakan suhu kesetimbangan. δ13C dan δ34S dari mineral karbonat dan sulfida yang hidup berdampingan dapat digunakan untuk menentukan pH dan fugasitas oksigen dari fluida pembawa bijih selama pembentukan bijih. Di sebagian besar ekosistem hutan, sulfat sebagian besar berasal dari atmosfer; pelapukan mineral bijih dan evaporit menyumbangkan belerang. Belerang dengan komposisi isotop yang khas telah digunakan untuk mengidentifikasi sumber polusi, dan belerang yang diperkaya telah ditambahkan sebagai perunut dalam studi hidrologi. Perbedaan kelimpahan alami dapat digunakan dalam sistem di mana terdapat cukup variasi dalam 34S komponen ekosistem. Danau Pegunungan Rocky diperkirakan didominasi oleh sumber sulfat atmosfer dan telah ditemukan memiliki nilai 34S karakteristik dari danau yang diyakini didominasi oleh sumber DAS sulfat. 35S yang radioaktif terbentuk dalam spalasi sinar kosmik 40Ar atmosfer. Fakta ini dapat digunakan untuk membuktikan adanya sedimen atmosfer baru-baru ini (tidak lebih dari 1 tahun) dalam berbagai hal. Isotop ini dapat diperoleh secara artifisial dengan berbagai cara. Dalam praktiknya, reaksi 35Cl + n → 35S + p, yang berjalan pada iradiasi kalium klorida oleh neutron, digunakan.[26] Isotop 35S digunakan dalam berbagai senyawa yang mengandung belerang sebagai pelacak radioaktif untuk banyak penelitian biologis, misalnya digunakan dalam percobaan Hershey–Chase. Bekerja dengan senyawa yang mengandung isotop ini relatif aman, asalkan senyawa tersebut tidak jatuh ke dalam organisme pelaku eksperimen.[27] Keterjadian alami     32S tercipta di dalam bintang masif, pada kedalaman yang suhunya melebihi 2,5×109 K, melalui fusi satu int silikon ditambah satu inti helium.[28] Karena reaksi nuklir ini merupakan bagian dari proses alfa yang menghasilkan unsur-unsur dalam kelimpahan, belerang adalah unsur paling umum ke-10 di alam semesta. Belerang, biasanya sebagai sulfida, terdapat dalam banyak jenis meteorit. Kondrit biasa mengandung rata-rata 2,1% belerang, dan kondrit karbon mengandung sebanyak 6,6%. Ia biasanya hadir sebagai troilit (FeS), tetapi terdapat pengecualian, dengan kondrit karbon yang mengandung belerang bebas, sulfat dan senyawa belerang lainnya.[29] Warna khas satelit vulkanis Jupiter Io dikaitkan dengan berbagai bentuk belerang cair, padat, dan gas.[30] Belerang adalah unsur paling umum kelima berdasarkan massa di Bumi. Belerang elemental dapat ditemukan di dekat mata air panas dan daerah vulkanis di banyak belahan dunia, terutama di sepanjang Cincin Api Pasifik; deposit vulkanis tersebut saat ini ditambang di Indonesia, Chili, dan Jepang. Endapan ini adalah polikristalin, dengan kristal tunggal terbesar yang terdokumentasi berukuran 22×16×11 cm.[31] Secara historis, Sisilia adalah sumber utama belerang pada Revolusi Industri.[32] Danau belerang cair dengan diameter hingga ~200 m telah ditemukan di dasar laut, terkait dengan gunung berapi bawah laut, pada kedalaman di mana titik didih air lebih tinggi daripada titik lebur belerang.[33] Belerang asli disintesis oleh bakteri anaerob yang bekerja pada mineral sulfat seperti gipsum dalam kubah garam.[34][35] Endapan yang signifikan dalam kubah garam terjadi di sepanjang pantai Teluk Meksiko, dan di evaporit di Eropa Timur dan Asia Barat. Belerang asli dapat diproduksi oleh proses geologi saja. Endapan belerang berbasis fosil dari kubah garam pernah menjadi basis produksi komersial di Amerika Serikat, Rusia, Turkmenistan, dan Ukraina.[36] Saat ini, produksi komersial masih dilakukan di tambang Osiek di Polandia. Sumber-sumber tersebut sekarang memiliki kepentingan komersial sekunder, dan sebagian besar tidak lagi berfungsi. Senyawa belerang alami yang umum ialah mineral sulfida, seperti pirit (besi sulfida), sinabar (raksa sulfida), galena (timbal sulfida), sfalerit (seng sulfida), dan stibnit (antimon sulfida); dan mineral sulfat, seperti gipsum (kalsium sulfat), alunit (kalium aluminium sulfat), dan barit (barium sulfat). Di Bumi, seperti di satelit Jupiter Io, belerang elemental terjadi secara alami dalam emisi vulkanis, termasuk emisi dari ventilasi hidrotermal. Sumber belerang industri utama sekarang adalah minyak bumi dan gas alam.[7] SenyawaKeadaan oksidasi belerang berkisar dari −2 hingga +6. Belerang membentuk senyawa yang stabil dengan semua unsur kecuali gas mulia. Reaksi transfer elektron Polikation belerang, S82+, S42+, dan S162+ dihasilkan ketika belerang direaksikan dengan zat pengoksidasi dalam larutan asam kuat.[37] Larutan berwarna yang dihasilkan dengan melarutkan belerang dalam oleum pertama kali dilaporkan pada tahun 1804 oleh C.F. Bucholz, tetapi penyebab warna dan struktur polikation yang terlibat baru ditentukan pada akhir 1960-an. S82+ berwarna biru tua, S42+ berwarna kuning, dan S162+ berwarna merah.[12] Reduksi belerang menghasilkan berbagai polisulfida dengan rumus Sx2-, banyak di antaranya telah diperoleh bentuk kristal. Ilustratif adalah produksi natrium tetrasulfida:
Beberapa dianion ini berdisosiasi menjadi anion radikal, seperti S3− yang memberi warna biru pada batu lapis lazuli.  Reaksi ini menyoroti sifat khas belerang: kemampuannya untuk mengatenasi (mengikat dirinya sendiri melalui pembentukan rantai). Protonasi anion polisulfida ini menghasilkan polisulfan, H2Sx dengan x= 2, 3, dan 4.[39] Pada akhirnya, reduksi belerang akan menghasilkan garam sulfida:
Interkonversi spesies ini dieksploitasi dalam baterai natrium–belerang. HidrogenasiPerlakuan belerang dengan hidrogen menghasilkan hidrogen sulfida. Ketika dilarutkan dalam air, hidrogen sulfida bersifat agak asam:[5]
Gas hidrogen sulfida dan anion hidrosulfida sangat beracun bagi mamalia, karena menghambat kapasitas pembawa oksigen dari hemoglobin dan sitokrom tertentu dengan cara yang analog dengan sianida dan azida (lihat di bawah, di bagian pencegahan). PembakaranDua oksida belerang utama diperoleh dengan membakar belerang:
Banyak oksida belerang lain yang teramati termasuk oksida kaya belerang seperti belerang monoksida, disulfur monoksida, disulfur dioksida, dan oksida yang lebih tinggi yang mengandung gugus perokso. HalogenasiBelerang bereaksi dengan fluorin menghasilkan belerang tetrafluorida yang sangat reaktif dan belerang heksafluorida yang sangat lengai.[40] Fluorin menghasilkan senyawa S(IV) dan S(VI), sementara klorin menghasilkan turunan S(II) dan S(I). Jadi, belerang diklorida, disulfur diklorida, dan klorosulfan yang lebih tinggi muncul dari klorinasi belerang. Sulfuril klorida dan asam klorosulfat adalah turunan dari asam sulfat; tionil klorida (SOCl2) adalah reagen umum dalam sintesis organik.[41] PseudohalidaBelerang mengoksidasi sianida dan sulfit untuk menghasilkan masing-masing tiosianat dan tiosulfat. Logam sulfidaBelerang bereaksi dengan banyak logam. Logam elektropositif menghasilkan garam polisulfida. Tembaga, seng, perak akan diserang oleh belerang, lihat menodai. Meskipun banyak logam sulfida yang diketahui, sebagian besar dibuat dengan reaksi suhu tinggi dari unsur-unsur tersebut.[42] Senyawa organik
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||



