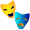Buchererova–Bergsova reakceBuchererova–Bergsova reakce je reakce karbonylových sloučenin (aldehydů nebo ketonů) či kyanhydrinů s uhličitanem amonným a kyanidem draselným za vzniku hydantoinů.[1][2][3][4] Tuto reakci objevil Hans Theodor Bucherer.  Mechanismus Kondenzací karbonylové sloučeniny s amonnou solí se vytvoří imin, který je poté atakován kyanidem za vzniku aminonitrilu. Nukleofilní adicí aminonitrilu na oxid uhličitý vznikne kyanokarbamová kyselina, jež projde vnitromolekulárním uzavřením kruhu, které utvoří 5-imino-oxazolidin-2-on. 5-imino-oxazolidin-2-on se přes isokyanát přesmykuje na hydantoin. HistorieReakce podobná Buchererově–Bergsově byla poprvé popsána na začátku 20. století, šlo o přípravu 5,5-dimethylhydantoinu ze směsi acetonu a kyanovodíku vystavené několik měsíců slunečnímu světlu. V roce 1929 byl zveřejněn postup přípravy řady 5-substituovaných hydantoinů; později bylo zjištěno, že reakci lze provést i za nižších teplot a tlaků a také že lze místo karbonylových sloučenin použít kyanhydriny. Následoval objev, že se dá jako velmi vhodné rozpouštědlo použít 50% ethanol. Roku 1934 byl navržen mechanismus reakce.[5] OmezeníJedním z omezení Buchererovy–Bergsovy reakce je to, že změny struktury produktů lze dosáhnout pouze změnou použitého ketonu či aldehydu. Tento nedostatek lze překonat přidáním 2-methylenaziridinu. Nejprve působením 2-methylenaziridinu 1, Grignardova činidla, měďné soli jako katalyzátoru, a R2-X dojde k otevření kruhu 2-methylenaziridinu za vzniku ketiminu 2. Ketimin následně reaguje se sloučeninami používanými při klasických Buchererových-Bergsových reakcích, čímž se vytvoří 5,5'- disubstituovaný hydantoin 3. Na strukturu produktu zde mají vliv tři látky: použitý aziridin, organokovové činidlo a elektrofil.[5]  VylepšeníBuchererovy–Bergsovy reakce lze podpořit použitím ultrazvuku. Buchererovy–Bergsovy reakce bývaly doprovázeny potížemi s polymerizací, dlouhými reakčními časy, a obtížným prováděním. Buchererovy–Bergsovy reakce využívající ultrazvuk mohou být použity na přípravu 5,5-disubstituovaných hydantoinů; takové reakce je možné také uskutečnit za nižších teplot, v kratších časech a s vyššími výtěžky.[6] ObměnyObdobami Buchererových–Bergsových reakcí jsou reakce karbonylových sloučenin se sirouhlíkem a kyanidem amonným v methanolu, kterými vznikají 2,4-dithiohydantoiny.[7] Reakcemi ketonů s monothiokarbamátem amonným a kyanidem sodným se vytvářejí 5,5-disubstituované 4-thiohydantoiny.[8]  StereospecifitaNěkdy mohou použité karbonylové sloučeniny vykazovat tak silné sterické efekty, že se vytváří jediný stereoisomer; většinou ale ke stereoselektivitě nedochází a oba stereoisomery se tvoří v poměru 1:1 Hydantoin vznikající Buchererovou–Bergsovou reakcí může být hydrolyzován na aminokyselinu; na následujícím obrázku je pro srovnání zobrazena také aminokyselina vznikající Streckerovou syntézou.[9]  VyužitíHydantoiny vytvořené Buchererovými–Bergsovými reakcemi lze využít:
OdkazyReferenceV tomto článku byl použit překlad textu z článku Bucherer–Bergs reaction na anglické Wikipedii.
Související článkyExterní odkazy
|